Нобелова награда
по Медицина или Физиология за 2010 г.
Резюме на официалния материал на Нобеловата фондация
Галина Сачанска
Нов Български Университет, 2011
„In vitro” оплождане при човека
Нобеловата награда по Медицина или Физиология за 2010 г. беше присъдена на английския учен Д-р Робърт Едуардс за разработването и внедряването на „in vitro” оплождането при човека. Значителна част от човечеството – около 10 % от двойките страдат от невъзможността да имат деца в резултат на репродуктивни несъвършенства.
През 50-те години на 20-ти век Едуардс стига до идеята да осъществи оплождане „в епруветка”. На това го навеждат резултатите от неговите изследвания върху контрола на яйчниковата функция при мишките под въздействие на различни полови хормони. Всички усилия на Едуардс се възнаграждават с успех в 23.47 ч на 25 Юли 1978 г., когато се ражда Луиза Браун – първото в света бебе, получено чрез „in vitro” оплождане.
В момента около 4 милиона бебета по света са родени с помощта на този метод.
Въведение
Проблемът с безплодието е сериозен и стресиращ за човешкия индивид, защото води до депресия, социална изолация и ниско качество на живот. В желанието си да преоделят това нещастие мнозина от тези двойки се подлагат на опасни манипулации в нерегламентирани медицински заведения, които са рискови за здравето, а дори и за живота им.
Невъзможността при жената да има деца най-често се дължи на увреждания на Фалопиевите тръби (яйцепроводите), което възпрепятства доближаването и сливането на яицеклетката и сперматозоида.
При мъжа невъзможността да има деца е свързана с количеството и качеството на семенната течност.
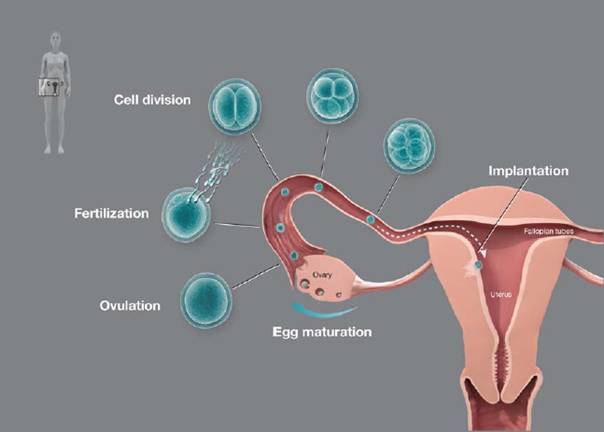
На фиг. 1 е представен процесът на оплождане при човека.
|
|
Фиг. 1 Процесът на оплождане при човека (по Nobel prize Foundation)
Женските полови клетки (гаметите) се съхраняват в яйчниците като отделни фоликули, които преминават през различни етапи при тяхното узряване – първичен, вторичен и третичен (зрял) фоликул. Зрелият фоликул е наречен още Граафово мехурче на името на холандеца Рене де Грааф, който пръв е установил етапите на развитие на половите клетки при женските бозайници.
Всеки един фоликул съдържа една полова клетка, обградена от няколко слоя гранулозни клетки. Всеки един женски индивид от бозайниците се ражда със начално количество неузрели яйцеклетки, намиращи се във фаза „Мейоза I”, и които узряват последователно през протежение на живота.
При наличие на бързо нарастващи концентрации на лутеинизиращия хормон (ЛХ), започва отключването на каскада от процеси, които водят до нарастване и узряване на женската яицеклетка, която се означава като ооцит.
Сперматозоидите от семенната течност, попаднала в матката се придвижват към далечния край на Фалопиевата тръба към освободената и попаднала в нея яйцеклетка. При успешно пробиване на дебелата обвивка на яйцеклетката от сперматозоида и навлизането на ядрото на сперматозоида в яйцеклетката става сливането на ядрата на двете полови клетки и намиращите се там хаплоидни набори хромозоми за всяка една от клетките. В резултат на това сливане се образува ембрион, които започва да се дели (етап „бластула”), пътувайки по протежението на Фалопиевата тръба към матката. В матката ембрионът се загнездва в повърхностният вътрешен слой на матката, наречен ендометриум. До края на ембрионалния период развитието именно на това място, като след определен период от време се образува плацентата.
„In vitro” оплождането най-напред е било изучено при видове, които не спадат към бозайниците – при морски животни, където опложадането става не вътрешно, а във външната среда. Първото описание на навлизане на сперматозоид в яйцеклетка е описано от Nelson (1851) при паразитиращите при човека кръгли червеи от род Ascaris. По-късно, през 1935 г. Грегъри Пинкус от Уорчестърската Фондация по Експериментална Биология, САЩ описва за първи път експерименталните условия за узряване на ооцити от заек „in vitro”, метафаза на мейоза II (Pincus, G. and Enzmann, E.V. , 1935). Колегата на Пинкус – Мин Чуен Чанг доказва през 1959 г., че е възможно оплождане на яйцеклетка от заек „in vitro”, при което се получават жизнени ембриони. Получените ембриони са имплантирани в женски заек, при което се родили жизнени малки зайчета (Chang, M.C., 1959). Изследователските резултатите на Чанг представляват значителен напредък за „in vitro” оплождането, но недостатъкът на метода е в необходимостта от предварителна преинкубация на заешките сперматозоиди в матката на женската. Причината за това е и, че Чанг не използва изцяло „in vitro”-условия. Причината за това е било ширещото по онова време схващане, че активирането на сперматозоидите може да се осъществи единствено “in vivo”. Чанг и неговият сътрудник Янагимачи доказват неправилността на тази догма, намирайки експериментални условия, при които е възможно активирането на сперматозоиди от хамстер извън живия организъм, и че те са способни да оплодят женската яйцеклетка. Полученият ембрион обаче доживявал само етап „2 клетки”.
„In vitro” оплождането при човека – едно монументално откритие
През първата половина на 20-ти век учените, изследващи оплождането започнали усилено да обсъждат възможностите за оплождане извън човешкия организъм. Съществен напредък в тази област бил постигнат едва през 60-те години. Тогава се установило, че за осъществяването на този процес са необходими:
- специфични технически средства
- контролиран процес на узряване на ооцитите и използване на ооцит в точно определен, подходящ за оплождане етап
- активиране на сперматозоидите „in vitro”
- изясняване на условията, които ще предизвикат оплодителен процес
- изясняване на оптималните условия за началното развитие на ембриона
- намиране на подходящ метод за поствяне на ембриона в матката на майката.
В края на 50-те години Робърт Едуардс, работейки в Националния Институт по Медицински изследвания в Лондон е бил посветен на развитието на методи за „in vitro” оплождането при човека. Едуардс притежавал изключително задълбочени познания по процеса на оплождане. Той получил изчерпателната си компетентност благодарение на многогодишни изследвания на върху репродуктивната система при животните и затова е бил добре подготвен за това предизвикателство. Едуардс знаел от работата на Пинкус, че ооцитите на бозайниците се нуждят само от няколко часа култивиране „in vitro” за да бъдат годни за оплождане. За период от няколко години Едуардс се опитва да намери подходящи условия за активиране нна спящите, неузрели ооцити. Неговите усилия се увенчават с успех през 1965-та година, когато той открива, че незрели човешки ооцити след 24-часова инкубация „in vitro” могат да встъпят в процес на узряване. (Edwards, 1965a, 1965b).
През 1969 г. студентът на Едуардс от Кембриджкия Университет, Великобритания Бари Бейвистър най-накрая успял да намери оптимален буфер, в който да се активират на сперматозоидите от семенна течност на хамстер в „in vitro” условия. Той също доказал, че активирани по този начин човешки сперматозоиди са годни да осъществят оплождане на активирани в „in vitro” условия човешки ооцити. Тези резултати представляват важно откритие и са крайъгълен камък в изследването на възпроизвеждането при човека. Те откриват пътя към развитието на метода за изкуственото оплождане.
Постигането на успеха
Робърт Едуардс открил, че въпреки, че човешките ооцити, които узряват „in vitro” могат да бъдат оплождани, получените ембриони преживяват само до етап „2 клетки”. Този резултат той отдал на факта, че ооцитите престояват прекалено дълго време извън тялото и решил да използва ооцити, които са завършили узряването си в тялото. Едуардс бил убеден, че ако е възможно да се извадят зрели ооцити от жената непосредствено преди тяхното отделяне от яйчника, те биха били далеч по-подходящи за оплождане „in vitro” и за ранното развитие на ембриона.
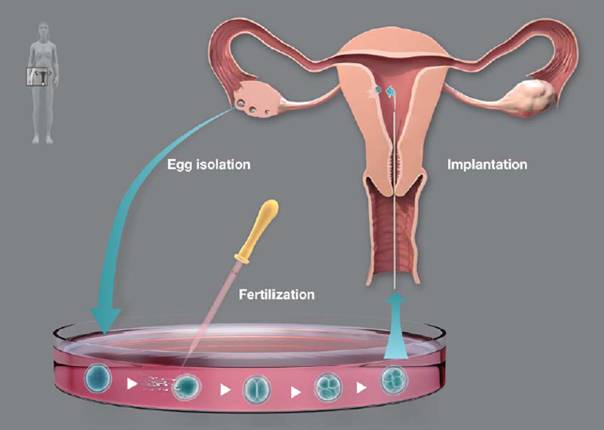
Ооцитите се отделят оперативно чрез лапароскопия от женския яйчник в етап „Метафаза на мейоза II”, непосредствено преди овулацията. Изолираните ооцити се поставят в петриева паничка с хранителна среда и сперматозоиди. Хранителната среда в петрито индуцира активиране на сперматозоидите „in vitro”, необходимо за оплождането. Съприкосновението яйцеклетка-сперматозоид подпомага мейозата на яйцеклетката, в резултат на което се получават два хаплоидни набора хромозоми. Единият от тези набори ще се слее с хаплоидния набор хромозоми на сперматозоида, а вторият ще бъде отделен в средата като второ полярно телце, съобразно с принципите на протичане на мейотичното делене.
|
|
Фиг. 2 Метод на „in vitro” оплождането, разработен от Едуардс (по Nobel prize Foundation)
Процесът на оплождане завършва с образуването на ембрион, които се дели до етап „8 клетки” (2.5 дни) в условията „in vitro”. 2.5 дни след оплождането ембрионът се прехвърля посредством тънка игла в матката на майката. В матката ембрионът ще се дели до достигането на етап „бластула”, след което ще се вгнезди (имплантитра) във вътрешния повърхностен слой на матката – ендометриума. По-нататъшното развитие на ембриона става именно там, а по-късно се образува и плацентата.
Новият метод на Едуардс почива на изследванията му върху репродуктивната биология на мишките. Той описва, че мейотичното узряване на ооцитите може да бъде стимулирано чрез допълнителни количества гонадотропни хормони, инжектирани в майката. Тези хормони наподобяват действието на синтезиращият се в организма лутеинизиращ хормон, които стимулира разпукването на зреещия фоликул т.е. овулацията.
В края на 60-те години на 20-ти век, отделянето на яйцеклетки от жената е ставало хирургически чрез отрязване на малка част от яйчника. Прочитайки научната статия на Д-р Патрик Стептоу Едуардс узнава за нов метод, наречен Лапароскопия (Steptoe, 1968). Лапароскопията е метод, който позволява наблюдението на женската полова система с помощта на нишковиден оптичен ендоскоп, въведен през малък отвор в близост до пъпа. Стептоу, който работи в Oldham and District General Hospital е опитен хирург и гинеколог, който въвежда лапароскопията във Великобритания и доказва, че чрез този метод могат да бъдат получени ооцити от яйчника.
Едуардс незабавно осъзнава, че този метод може да бъде използван за получаване на ооцити във фаза „Метафаза на мейоза II” в пододящ момент от менструалния цикъл. Той се свързва със Стептоу и през 1970 г. двамата доказват, че след терапия с гонадотропни хормони е възможно чрез лапароскопски да се извадят от женски яйчник ооцити във фаза „Метафаза на мейоза II”.
В публикация от 1970 г. съавторите описват, че са извършили „in vitro” оплождане с предовулационни ооцити и „in vitro” активирани сперматозоиди, като полученият ембрион преживява вече етапа „8 клетки”.
Откритието е епохално в два аспекта:
- За първи път е показано, че „in vitro” активирана семенна течност е способна да доведе до развитие на ембрион до етап, по-дълъг от „2 клетки” при бозайници
- За първи път е показано, че човешки ембрион може да се дели „in vitro”.
|
|
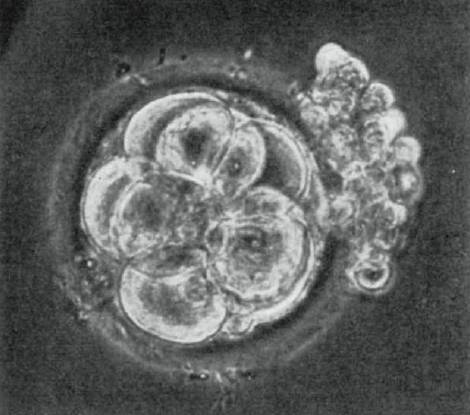
Фиг. 3 Фотография на ембрион на етап „8 клетки”, получен при „in vitro”оплождане (Снимка от публикация на Р. Едуардс в сп. Nature (1970); По Nobel Prize Foundation)
В началото на 70-те години, Едуардс и Стептоу започват да имплантират ранни ембриони, получени по „in vitro” метода в жени. След около 100 опита, които достигат едва до краткотрайна бременност те осъзнават, че хормоналната терапия, на която са били подложени жените за получаване на ооцити препятства развитието на ембриона в матката и води до спонтанни аборти.
След промяна в схемата на хормоналаната терапия през 1976 г. се стига до успешна бременност. За съжаление тази бременност е трябвало да бъде прекъсната, тъй като ембрионът се имплантирал неподходящо във Фалопиевата тръба на пацентката.
Тогава Едуардс и Стептоу решават да се откажат от хормоналаната терапия при изваждане на яйцеклетки и да се осланят само на естествения меструален цикъл на пациентките, въпреки, че това означавало, че могат да получат само една яйцеклетка за цикъл. Благодарение на данните за концентрацията на Лутеинизиращия хормон в урината на пациентките те могли да предположат кога евентуално узряващият ооцит ще достигне фаза „Метафаза на мейоза II” “in vivo”. Двамата учени се надявали да успеят да получат яйцеклетката чрез лапароскопия преди овулацията.
Р. Едуардс и П. Стептоу успяват и техните усилия се увенчават с успех, когато през 1978 г. правят историческото съобщение, че нормално и здраво бебе - Луиза Браун се е родило чрез успешно „in vitro” оплождане на човешки ооцити (Steptoe and Edwards, 1978, www.youtube).
Най-накрая дългосрочната визия на Едуардс се сбъдва, отвяряйки нова ера при третирането на безплодието.
Текстът на писмото до Издателя на списание „Lancet” документира раждането на първото „бебе в епруветка”.
|
Letters to the Editor
BIRTH AFTER THE REIMPLANTATION OF A HUMAN EMBRYO
SIR, — We wish to report that one of our patients, a 30-year-old nulliparous married women, was safely delivered by cæsarean section on July 25, 1978, of a normal infant girl weighing 2700 g. The patient had been referred to one of us (P.C.S) in 1976 with a history of 9 years’ infertility, tubal occlusions, and unsuccessful salpingostomies done in 1970 with excision of the ampullæ of both oviducs followed by persistent tubal blockages. Laparoscopy in February, 1977, revealed grossly distorted tubal remnants with occlusion and peritubal and ovarian adhesions. Laparotomy in August, 1977, was done with excision of the remains of both tubes, adhesolysis, and suspension of the ovaries in good position for oocyte recovery. Pregnancy was established after laparoscopic recovery of an oocyte on Nov. 10, 1977, in-vitro fertilization and normal cleavage in culture media, and the reimplantation of the 8-9 cell embryo into the uterus 21/2 days later. Amniocentesis at 16 weeks’ pregnancy revealed normal α-fetoprotein levels, with no chromosome abnormalities in a 46 XX fetus. On the day of delivery the mother was 38 weeks and 5 days by dates from her last menstrual period, and she had pre-eclamptic toxæmia. Blood-pressure was fluctuating around 140/95, oedema involved both legs up to knee level together with the abdomen, back, hands, and face; the blood-uric-acid was 390 μmol/l, and albumin 0·5 g/l of urine. Ultrasonic scanning and radiographic appearances showed that the fetus had grown slowly for several weeks from week 30. Blood-oestriols and human placental lactogen levels also dropped below the normal levels during this period. However, the fetus grew considerable during the last 10 days before delivery while placental function improved greatly. On the day of delivery the biparietal diameter had reached 9·6 cm, and 5 ml of amniotic fluid was removed safely under sonic control. The lecithin: sphingomyelin ratio was 3·9:1, indicative of maturity and low risk of the respiratory-distress syndrome. We hope to publish further medical and scientific details in your columns at a later date.
Department of Obstetrics and Gynæcology, General Hospital, Oldham OL1 2JH,P. C. STEPTOE University Physiology Laboratory, Cambridge CB2 3EG R. G. EDWARDS |
Фиг. 4 Копие на писмото до издателя на сп. “Lancet” (По Nobel Prize Foundation)
По-нататъшно развитие на “in vitro” оплождането
След раждането на Луиза Браун Едуардс и Стептоу основават Клиника за “in vitro” оплождане в Bourn Hall, Кеймбрижд, Великобритания, където продължават да развиват и усъвършенстват “in vitro” оплождането.
Именно в тази клиника се раждат второто и третото „бебе в епруветка”, а двамата учени въвеждат модификации на хормоналната терапия за стимулиране на яйчниците и култивирането на ембрионите. В резултат на тези подобрения през 1983 г. се раждат 183 бебета, и 1 000 - през 1986 г.Успоредно, в цял свят новата технология бързо се налага и през 1986 г. са родени общо 1 000 бебета. Първата генерация от тези бебета в момента е в репродуктивна възраст - малко над 30 години. Някои от тези жени вече имат деца по естествен път, без да използват “in vitro” оплождането.
Големите успехи привличат в последствие и други учени, които се посвещават на “in vitro” оплождането. По-късно е разработен и метода за микроинжектирането на сперматозоида вътре в цитоплазмата на ооцита, което е голям успех при третирането на мъжкото безплодие. С течение на времето е въведена и предимплантационната генетична диагностика. Тя се осъществява както “in vitro”, така и “in vivo” с цел предпазване от риск за хромозомни аномалии или генетични заболявания.
Здравен статус на родените чрез “in vitro” оплождане
Родените чрез изкуствено опождане деца са здрави както децата, заченати по естествен път. Това е доказано чрез редица изследвания (Basatemur and Sutcliffe, 2008;de Mouzon et al., 2009).
Етични аспекти
С въвеждането на “in vitro” оплождането възникват множество важни биоетични въпроси. Едуардс заедно с адвоката Дейвид Шарп написват материал, който инициира дебат по много и сложни теми и казуси, възникнали във връзка с репродуктивната медицина. Те настояват изследванията с човешките полови клетки и ембриони да се осъществява при пълна конфиденциалност и под съобразно стриктни биоетични указания.
По време на този дебат Едуардс и неговите съмишленици се сблъскват с острото отричане на метода за изкуствено оплождане от църквата. Според нейните водачи всичко свързано с тази технология е неморално. Опозиционни настроения са показани и от правителството на Великобритания, което счита, че е по-важно да се ограничи раждаемостта, вместо да се третира безплодието. На трето място се противопоставят научните колеги на Едуардс, чиято критичност се основава на начините за съхранение на ембриона. Именно този аргумент е бил посочен от Съвета за Медицински изследвания при отказа на проект, посветен на “in vitro” оплождането и депозиран през 1971 г. от Едуардс и Стептоу.
Удивителното е, че Едуардс не само, че отговаря на непрестанните критики на всички свои опоненти, но и успява да устои и да осъществи своята научна идея.
Заключение
Откриетието на Робърт Едуардс е колосално постижение в медицината, за което истински може да бъде казано, че има ”огромна полза за човечеството”. Това откритие радикално променя областта на репродуктивната медицина. Днес, между 2 и 3 % от всички новородени в много страни са заченати с помощта на “in vitro” оплождането. Този метод отвори нови пътища за преодоляване не само на женското, но и на мъжкото безплодие.
Нобеловият Комитет счита, че технологията за “in vitro” оплождане е докоснала и повлияла живота на милиони бездетни хора по света, давайки им възможност да имат деца и удостоява Робърт Едуардс с Нобеловата награда по Медицина или Физиология за 2010.
Патрик Стептоу умира през 1988 г. в Англия.
По материала на Christen Hoog,
Професор по Клетъчна биология, Каролинска Институт, Стокхолм,
Член на Нобеловия Комитет
Литературни източници
1. Pincus, G. and Enzmann, E.V. (1935), The comparative behavior of mammalian eggs in vivo and in vitro: I. The activation of ovarian eggs. J. Exp. Med. 62: 665-675.
2. Chang, M.C. (1959) Fertilization of rabbit ova in vitro. Nature. 184:466-675.
3. Edwards, R.G. (1965a) Maturation in vitro of mouse, sheep, cow, pig, rhesus monkey and human ovarian oocytes. Nature, 183:1744-1745.
4. Edwards, R.G. (1965b) Maturation in vitro of human ovarian oocytes. The Lancet, 2: 926-929.
5. Steptoe, P.C. (1968) Laparoscopy and ovulation. Lancet ii, 913.
6. Steptoe, P.C. and Edwards, R. G. (1978) Birth after the reimplantation of a human embryo. Lancet, 2: 366.
7. Basatemur, E and Sutcliffe, A. (2008) Follow-up of children born after ART. Placenta, 29: 135-140.
8. International Committee for monitoring assisted reproductive technology (ICMART): de Mouzon, J., Lancaster, P., Nygren, K., Sullivan, E., Zegers-Hochschild, F., Mansour, R., Ishiara, O. and Adamson, D. (2009) World collaborative report on assisted reproductive technology, 2002. Hum Reprod. 24: 2310-2320.
9. Nobel Prize Foundation